-
11 April 2024 750 000$ amassés lors du Gala Audace de l’IRIC de l’Université de Montréal
Le 10 avril dernier, plus de 250 convives se sont réunis pour le Gala Audace 2024 de l’IRIC. Grâce à la générosité des donateur(rice)s et des invité(e)s, un montant de 750 00 $ a été amassé. Depuis 2014, ce sont plus de 8 millions de dollars qui ont été récoltés à l’occasion du Gala Audace, permettant de pérenniser la recherche fondamentale réalisée à l’IRIC et de perfectionner les thérapies contre le cancer.
![]()
-
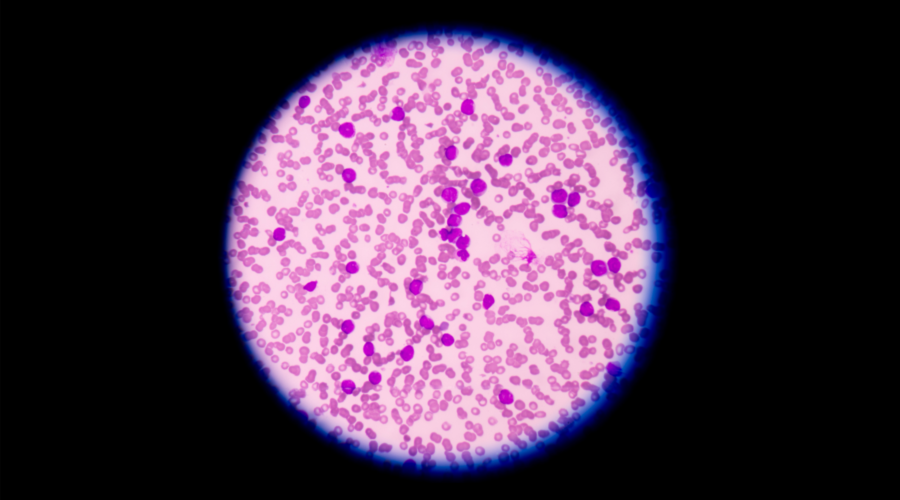
25 March 2024 Une nouvelle stratégie basée sur la surdose de cuivre pour traiter la LMA
Malgré les avancées thérapeutiques des dernières années dans le traitement de la leucémie myéloïde aiguë (LMA), cette pathologie reste associée à un mauvais pronostic. Dans une nouvelle étude, le groupe Leucegene dirigé par Guy Sauvageau, directeur de l’Unité de recherche en génétique moléculaire des cellules souches de l’IRIC, Anne Marinier, directrice de l’Unité de découverte du médicament de l’IRIC, et Josée Hébert (Banque de cellules leucémiques du Québec (BCLQ), Centre de recherche de l’Hôpital Maisonneuve-Rosemont) propose une stratégie thérapeutique basée sur la surdose de cuivre comme traitement d’un sous-groupe génétique de LMA particulièrement sensible à cette approche. Mené par Céline Moison et Deanne Gracias pour la biologie, et Julie Schmitt et Réjean Ruel pour la chimie, en collaboration avec l’équipe du laboratoire de génétique de la BCLQ, ce projet fait l’objet d’une publication dans le prestigieux journal Science Advances.
![]()
-
21 March 2024 Des honneurs de la SCBM pour Sylvie Mader et Guy Sauvageau
L’IRIC félicite Sylvie Mader et Guy Sauvageau, récipiendaires de prix de Société canadienne pour les biosciences moléculaires (SCBM). Sylvie Mader, directrice de l’Unité de recherche en ciblage moléculaire dans le traitement du cancer du sein de l’IRIC, est la lauréate 2024 du Prix de conférence d’honneur Jeanne Manery-Fisher. Guy Sauvageau, directeur de l’Unité de recherche en génétique moléculaire des cellules souches, est quant à lui récipiendaire de la médaille d’or Arthur-Wynne.
![]()
-
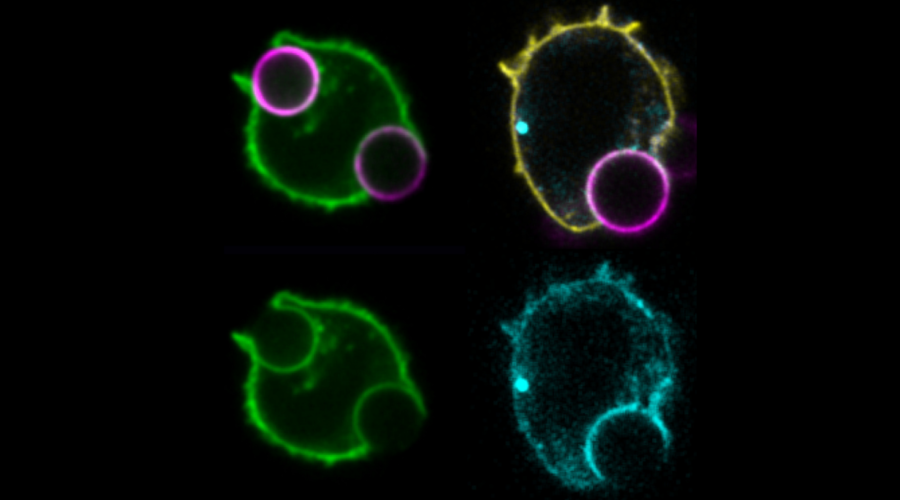
5 March 2024 Identification d’une activité enzymatique requise pour la complétion de la division cellulaire
La division cellulaire, processus requis pour la survie de toutes les espèces, permet de séparer le matériel génétique d’une cellule mère et de le partager entre ses deux cellules filles. Plusieurs aspects de la division cellulaire demeurant mal compris à ce jour, l’équipe de Jean-Claude Labbé, directeur de l’Unité de recherche en division et différenciation cellulaire, s’est penchée sur l’une de ses dernières étapes, la cytocinèse. L’équipe a identifié une nouvelle protéine, OSGN-1, comme étant requise pour la complétion correcte de la division cellulaire. L’étude, publiée dans le journal PNAS, a été menée par l’associée de recherche Eugénie Goupil et l’étudiante au doctorat Léa Lacroix.
![]()
-
20 February 2024 L’IRIC souligne la Journée internationale des femmes et filles de science
Le 10 février dernier, l’IRIC était présent au Centre des sciences de Montréal pour la journée Femmes et filles de Science à l’occasion de la Journée internationale des femmes et des filles de science. Cette 7e édition de l’événement a attiré une foule record, avec plus de 3300 curieux et curieuses au rendez-vous pour découvrir différentes disciplines scientifiques.
![]()
-
5 February 2024 Pasquale Gentile: « Sans la science, je n’aurais pas survécu à mon cancer. »
Dans la foulée du 4 février, Journée mondiale contre le cancer, visionnez le témoignage de Pasquale Gentile, un patient ayant reçu la thérapie cellulaire UM171.
![]()
-
1st February 2024 La Société canadienne du cancer octroie une subvention à Geneviève Deblois
Geneviève Deblois, directrice de l’Unité de recherche sur les mécanismes épigénétiques et métabolisme du cancer de l’IRIC, est récipiendaire d’une Subvention de recherche pour chercheuses et chercheurs prometteurs de la Société canadienne du cancer (SCC). Lors du concours 2023, seize de ces subventions ont été accordées au pays pour faire progresser les programmes de recherche en cancérologie. Seule chercheuse financée au Québec, Geneviève Deblois obtient un financement de 550 000 $ pour son projet « Trouver de meilleures façons de traiter le cancer du sein triple négatif ».
![]()
-
29 January 2024 Expansion des cellules souches hématopoïétiques : le mécanisme d’action de la molécule UM171 implique une régulation de la protéine MYC
L’expansion ex vivo de cellules souches hématopoïétiques (CSH), une avancée importante pour les thérapies cellulaires, peut entraîner des stress réplicatifs et métaboliques; un peu comme le fait le vieillissement. Dans ses efforts pour identifier les meilleures stratégies d’expansion des CSH, l’équipe de Guy Sauvageau, directeur de l’Unité de recherche en génétique moléculaire des cellules souches de l’IRIC, s’est penchée sur les mécanismes moléculaires induits pas la molécule UM171. Celle-ci, découverte conjointement en 2014 par son laboratoire et celui de Anne Marinier, directrice de l’Unité de découverte de médicaments de l’IRIC, permet l’expansion ex vivo des CSH dérivées du sang de cordon ombilical. Leur plus récente étude, menée par la chercheuse Jalila Chagraoui et publiée dans le journal Blood, rapporte que la molécule UM171 préserve les CSH du stress induit par la culture cellulaire en modulant l’activité de la protéine MYC.
![]()
-
25 January 2024 Décoder les bases moléculaires et structurales de la transduction de signaux pour concevoir des médicaments plus performants
Les récepteurs couplés aux protéines G (RCPG) sont liés par une panoplie de ligands : plus de 500 molécules présentes naturellement chez l’humain (comme les hormones) ainsi que le tiers des médicaments approuvés les ciblent. La liaison de ces ligands aux RCPG entraîne l’activation sélective de différentes voies de signalisation, qui sont impliquées dans des processus aussi variés que le métabolisme, la croissance cellulaire et les réponses immunitaires. Michel Bouvier, directeur de l’Unité de recherche en pharmacologie moléculaire et directeur général de l’IRIC, et ses collaborateurs ont voulu mieux comprendre, à l’échelle atomique, les déterminants moléculaires et structuraux qui dictent la capacité d’un ligand à activer un RCPG. Le travail, une collaboration avec Madan Babu, chercheur au Ste-Jude Research Hospital, et Brian Kobilka, chercheur à Stanford University et co-lauréat du prix Nobel de chimie 2012, a été mené par Franziska Heidenreich alors qu’elle était postdoctorante dans le laboratoire Bouvier. Il fait l’objet d’une publication dans le journal Science.
![]()
-
23 January 2024 Une colle moléculaire qui favorise la dégradation de la cycline K
Les protéines CDK12 et cycline K forment un complexe jouant des rôles importants dans plusieurs types de cancers, notamment les mélanomes et les cancers du sein. L’équipe de Philippe Roux, directeur scientifique et directeur de l’Unité de recherche en signalisation cellulaire et protéomique de l’IRIC, a caractérisé le mode d’action d’un nouvel inhibiteur de CDK12, développé pour son potentiel thérapeutique anticancer. Les résultats obtenus révèlent que l’inhibiteur en question, la molécule SR-4835, agit comme colle moléculaire pour induire la dégradation de la cycline K et ainsi inactiver le complexe qu’elle forme avec CDK12. Mené conjointement par les postdoctorants Thibault Houles et Jonathan Boucher, le projet fait l’objet d’une publication dans le journal Cell Death Discovery.
![]()
-
15 January 2024 Retour sur le 20e anniversaire de l’IRIC : Une année de célébration!
Au cours de ses 20 dernières années, l’IRIC a bâti un modèle de recherche unique au pays et rassemblé des expertises exceptionnelles. Afin de mettre en lumière sa communauté, de faire rayonner la science et de mettre la table sur les réalisations à venir, l’Institut a créé une programmation spéciale qui s’est échelonnée sur l’année 2023. Voici, en rétrospective, les différentes initiatives et célébrations qui ont su marquer cette année spéciale.
![]()
-
10 January 2024 Une nouvelle étude identifie des cibles pour l’immunothérapie dans deux sous-types de cancer du sein
Le cancer du sein est le cancer le plus répandu dans le monde. Il se présente en plusieurs sous-types qui diffèrent d’un point de vue immunologique; certains génèrent des réponses immunitaires plus fortes que d’autres. L’équipe de Claude Perreault, directeur de l’Unité de recherche en immunobiologie de l’IRIC, a utilisé une approche de protéogénomique pour étudier l’immunopeptidome de deux sous-types de cancer du sein : les cancers du sein à récepteurs hormonaux positifs et les cancers du sein triples négatifs. Ils ont ainsi identifié plusieurs nouveaux antigènes pour chaque sous-type, lesquels se sont par ailleurs révélés capables de générer une réponse immunitaire in vitro. Ces nouveaux antigènes représentent donc des cibles potentielles pour l’immunothérapie anticancéreuse. Le projet a été mené par la doctorante Eralda Kina et fait l’objet d’une publication dans The Journal of Clinical Investigation.
![]()
-
20 December 2023 Un financement de 6M$ pour améliorer le traitement de la leucémie myéloblastique aiguë
Guy Sauvageau, à titre de directeur de l’Unité de recherche en génétique moléculaire des cellules souches de l’IRIC, et Anne Marinier, à titre de directrice générale de la société biotechnologique RejuvenRx, obtiennent 6M $ sur 3 ans de Génome Canada pour le projet « Mise au point d’un nouvel outil de dégradation de la cycline-K pour les patients atteints de LMA à haut risque et caractéristiques génomiques connexes ». Le financement est octroyé dans le cadre du Programme de partenariats pour les applications de la génomique de Génome Canada, qui vise à favoriser les partenariats entre l’industrie, des utilisateurs publics, et la recherche académique.
![]()
-
15 December 2023 Deux lauréates des Bourses de recherche au doctorat de la SRC à l’IRIC!
L’IRIC tient à féliciter Myriam Iliana Ibanez Rios et Karla Lucia Paez Martinez pour l’obtention de leur Bourse de recherche au doctorat de la Société de recherche sur le cancer (SRC). Elles comptent parmi les 21 récipiendaires de ces nouvelles bourses, qui offrent un financement de 70 000 $ sur deux ans. Cette nouvelle initiative de la SRC vise à apporter un soutien essentiel à la communauté doctorale.
![]()
-
14 December 2023 Deux récipendaires des bourses d’excellence de l’UdeM parmi notre communauté étudiante!
Le Vice-rectorat adjoint aux études supérieures et postdoctorales a souligné l’excellence étudiante par la remise de 155 bourses. Deux membres de l’IRIC comptent parmi les récipiendaires de ces bourses d’excellence. Les bourses sont octroyées en fonction de la qualité du dossier scolaire, de la persévérance et de l’engagement bénévole des candidats et candidates.
![]()
-
1st December 2023 Les piliers de l’IRIC : rencontrez Mélanie Fréchette
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Mélanie Fréchette, technicienne en santé animale pour le laboratoire de Guy Sauvageau.
![]()
-
1st December 2023 Les piliers de l’IRIC : rencontrez Sandra Weber
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Sandra Weber, conseillère à la recherche dans le laboratoire de Marc Therrien à l’IRIC.
![]()
-
27 November 2023 Les piliers de l’IRIC : rencontrez Jinny Émond
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Jinny Émond, préposée aux soins animaliers pour la plateforme de biologie in vivo.
![]()
-
31 October 2023 Une subvention de la SRC pour valider des cibles thérapeutiques dans le cancer du foie
L’équipe de Sylvain Meloche, directeur de l’Unité de recherche en signalisation et croissance cellulaire de l’IRIC, a obtenu une subvention de 125 000 $ pour deux ans pour le projet « Validation préclinique des tyrosine kinases de la famille SRC comme cibles thérapeutiques dans le cancer du foie ». Cet octroi est financé en partenariat avec la Fondation canadienne du foie.
![]()
-
31 October 2023 Lucyle Depoërs, doctorante et vulgarisatrice scientifique, présente le magazine l’ÉclairSci
L’IRIC est fier de soutenir la création du nouveau magazine l’ÉclairSci. Initié par la doctorante Lucyle Depoërs, du laboratoire de Claude Perreault, le projet présentera sous forme d’infographies vulgarisées des études scientifiques réalisées par des équipes de l’IRIC. Sous forme digitale, l’ÉclairSci se veut accessible à tous et toutes afin de partager les plus récentes avancées en cancérologie au grand public.
![]()
-
30 October 2023 Une nouvelle plateforme pour prédire la sécurité de composés médicamenteux
De par leur capacité d’activation de multiples voies de signalisation à différents endroits dans la cellule, les récepteurs couplés au protéines G (RCPG) sont des cibles de choix dans le développement de médicaments. Shane C. Wright, de l’Institut Karolinska en Suède, a réussi à exploiter une nouvelle technologie développée pendant son postdoctorat dans le laboratoire de Michel Bouvier, directeur général et directeur de l’Unité de recherche en pharmacologie moléculaire de l’IRIC, et qui pourrait être utilisée afin de prédire les effets indésirables de nouveaux traitements avant leur utilisation en clinique. L’étude, fruit de la collaboration des équipes suédoise et montréalaise, fait l’objet d’une publication dans le journal Nature Communications.
![]()
-
27 October 2023 Succès pour le symposium de l’IRIC 2023!
Les 19 et 20 octobre derniers, plus de 250 convives se sont réunis à l’occasion du symposium scientifique international de l’IRIC. L’événement était également l’occasion pour tous et toutes de souligner officiellement le 20e anniversaire de l’IRIC, à l’Université de Montréal.
![]()
-
27 September 2023 13 000$ amassés dans le cadre du Marathon Beneva de Montréal
Les 23 et 24 septembre derniers avait lieu le Marathon Beneva de Montréal et l’IRIC est fier d’avoir collecté plus de 13 000$ grâce aux généreux donateurs et donatrices.
![]()
-
26 September 2023 Célébration du 20e de l’IRIC et de sa communauté!
Le 18 septembre dernier, 300 personnes de la communauté étudiante et du personnel employé de l’IRIC se sont assemblées pour célébrer le 20e anniversaire de l’Institut.
![]()
-
20 September 2023 Annonce des récipiendaires du concours Science Réflexion 2023
L’IRIC a le plaisir de vous annoncer les noms des gagnants et gagnantes du concours Science Réflexion 2023. Ce concours annuel permet de mettre en lumière la créativité et le talent de la communauté de l’IRIC et de présenter la science sous un autre angle.
![]()
-
19 September 2023 Félicitations aux trois récipiendaires du Concours de Bourses salariales de l’IRIC
Trois membres de la communauté postdoctorale de l’IRIC ont remporté le Concours de bourses salariales de l’IRIC cette année. Ces bourses ont été remises grâce à l’engagement de donateurs fidèles.
![]()
-
7 September 2023 IRIC sur la route : une tournée de recrutement étudiant propulsée par l’équipe des affaires académiques
Dans le cadre de sa tournée de recrutement étudiant IRIC sur la route, l’équipe des affaires académiques de l’Institut participera cet automne à plusieurs salons d’études supérieures organisés par des universités canadiennes.
![]()
-
6 September 2023 Pasquale Gentile : un patient traité avec la molécule UM171 en visite à l’IRIC
Le 14 juillet dernier, Pasquale Gentile, un patient ayant reçu la thérapie d’expansion cellulaire basée sur la molécule UM171, était de passage dans les laboratoires de l’IRIC afin de visiter l’Unité de découverte de médicaments et de rencontrer Stéphane Gingras, le chimiste ayant synthétisé la molécule UM171
![]()
-
6 September 2023 KIF18A : une cible anticancer prometteuse pour des thérapies de combinaison avec des inhibiteurs de PLK1
La kinase PLK1 est impliquée à plusieurs niveaux dans le contrôle de la division cellulaire. Les cellules cancéreuses sont souvent particulièrement dépendantes de l’activité de cette enzyme. Les thérapies anticancer développées pour cibler PLK1 demeurent toutefois peu efficaces à ce jour. Le laboratoire du professeur Vincent Archambault, directeur de l’Unité de recherche sur la régulation du cycle cellulaire de l’IRIC, a collaboré avec le laboratoire du professeur Michael Tyers, alors directeur de l’Unité de recherche en biologie des systèmes et biologie synthétique, pour mieux comprendre les fonctions cellulaires de PLK1 et identifier des gènes dont l’inactivation interfère avec la prolifération cellulaire en synergie avec des inhibiteurs de PLK1 existants. Les résultats obtenus suggèrent que l’inhibition de la kinésine KIF18A pourrait s’avérer une avenue thérapeutique à exploiter en combinaison avec des inhibiteurs de PLK1. Publiée dans le journal PLOS Genetics, l’étude a été menée par la conseillère à la recherche Karine Normandin.
![]()
-
24 August 2023 Capitaine Mathilde : conjuguer course et science au profit de la recherche
Conseillère à la recherche dans le laboratoire de Sylvain Meloche, qui dirige l’Unité de recherche en signalisation et croissance cellulaire, Mathilde Soulez a accepté pour une deuxième année consécutive d’enfiler le dossard de capitaine de l’Équipe IRIC dans le cadre du Marathon Beneva de Montréal. Scientifique, coureuse, entraîneuse, maman; entretien avec une femme aux talents et intérêts multiples.
![]()
-
24 August 2023 Les piliers de l’IRIC : rencontrez Madeleine Héroux
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, faites la rencontre de Madeleine Héroux, directrice adjointe – biologie de l’Unité de découverte du médicament.
![]()
-
18 August 2023 La Journée des stagiaires d’été de l’IRIC 2023 : L’occasion de s’initier à la communication scientifique
La cinquième édition de la Journée des stagiaires d’été de l’IRIC s’est tenue le jeudi 10 août dernier. L’événement, organisé par le Bureau des affaires académiques de l’IRIC de pair avec des stagiaires d’été a permis à 11 stagiaires de s’initier à la communication scientifique devant leurs pairs et leurs collègues de l’IRIC. Un total de quatre présentations orales et de sept présentations par affiches a été mis en œuvre.
![]()
-
2 August 2023 Les piliers de l’IRIC : rencontrez Simon Girard
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Simon Girard, conseiller à la recherche dans le laboratoire de Guy Sauvageau à l’IRIC.
![]()
-
1st August 2023 Identification de la protéine Emerin comme cible de la phosphatase PP2A-B55 : une régulation clé pour la sortie de mitose
L’Unité de recherche sur la régulation du cycle cellulaire et l’Unité de recherche en protéomique et spectrométrie de masse de l’IRIC, dirigées respectivement par les professeurs Vincent Archambault et Pierre Thibault, ont tiré avantage de la mouche à fruits Drosophila melanogaster pour identifier des protéines cibles de PP2A-B55. Leurs résultats révèlent que la protéine de l’enveloppe nucléaire Emerin est déphosphorylée par PP2A-B55; une régulation importante pour la reformation de l’enveloppe nucléaire et le développement embryonnaire. Menée conjointement par les doctorantes Virginie Emond-Fraser et Myreille Larouche, l’étude fait l’objet d’une publication dans le journal Open Biology de la Royal Society.
![]()
-
24 July 2023 Quatre équipes de l’IRIC obtiennent du financement des Instituts de recherche en santé du Canada
Les Instituts de recherche en santé du Canada (IRSC) ont récemment attribué les subventions du programme Projet pour le concours du printemps 2023. Ce programme vise à soutenir les idées originales ayant le potentiel de faire avancer les connaissances fondamentales et appliquées en santé. Au pays, ce sont 381 projets de recherche, représentant un investissement total de 325 millions de dollars, qui ont été financés. Quatre projets de l’IRIC sont récipiendaires de ces prestigieux octrois.
![]()
-
19 July 2023 École d’été de l’UdeM : une opportunité pour la relève de s’initier à la biologie moléculaire dans nos laboratoires
Dans le cadre de l’École d’été de l’Université de Montréal, 8 jeunes de 15 à 17 ans ont pu participer le 4 juillet dernier à un atelier thématique dans les laboratoires de l’IRIC. Animé par les étudiantes au doctorat Fadia Boudghene-Stambouli, Eloïse Duramé et Chloé Tesnière, l’atelier d’une demi-journée leur a permis d’expérimenter pour apprendre sur la biologie moléculaire et la cancérologie.
![]()
-
6 July 2023 Identification d’une nouvelle voie pro-motilité impliquant la protéine CNK2 dans les cellules cancéreuses
À l’IRIC, Marc Therrien et son équipe cherchent à comprendre comment la transduction des signaux est perturbée dans les cellules cancéreuses, leur permettant de se diviser et de se propager dans l’organisme même en l’absence des signaux appropriés. Le projet dirigé par les doctorants Jessica Gagnon et Guillaume Serwe, et l’associé de recherche David Kachaner, a été publié dans le journal Nature Communications et décrit une nouvelle voie de signalisation dans laquelle la protéine d’échafaudage CNK2 joue un rôle central pour l’augmentation de la motilité des cellules cancéreuses. Les équipes de recherche de Gregory Emery et Sylvain Meloche à l’IRIC ont également contribué à cette étude.
![]()
-
5 July 2023 Visitez la nouvelle boutique IRIC !
L’IRIC est fier de lancer sa nouvelle boutique en ligne. Que ce soit pour un événement sportif ou simplement au quotidien, faites rayonner l’Institut en portant ses couleurs.
![]()
-
5 July 2023 La Société de leucémie et lymphome du Canada remet deux prix nommés en l’honneur de membres de l’IRIC
La Société de leucémie et lymphome du Canada (SLLC) remet chaque année six prix mettant en lumière les contributions des bénévoles et du personnel de l’organisation. Deux de ces prix ont été nommés en l’honneur de membres de l’IRIC : le Prix Dre Trang Hoang – Professionnel(le) de la santé de l’année et le Prix William Brock – Courage et inspiration. L’IRIC est très fier de pouvoir compter au quotidien sur ces deux modèles d’engagement.
![]()
-
4 July 2023 ENPP1 réduit la réponse immunitaire dans les cancers du sein HER2+
HER2∆16 est un variant oncogénique du récepteur du facteur de croissance épidermique humain (HER2); il est impliqué dans les cancers du sein et d’autres types de tumeurs comme moteur de la tumorigenèse et du processus métastatique. Le laboratoire du professeur Philippe Roux, directeur de l’Unité de recherche en signalisation cellulaire et protéomique de l’IRIC, a collaboré avec l’équipe de William Muller, de l’Institut de cancer Rosalind et Morris Goodman de l’Université McGill, pour caractériser les mécanismes moléculaires sous-jacents de l’oncogénicité médiée par HER2Δ16. Les résultats obtenus suggèrent que HER2Δ16 altère le microenvironnement tumoral via la protéine ENPP1, qui pourrait s’avérer être une cible thérapeutique intéressante. Publiée dans le journal Cancer Immunology Research, l’étude a été menée conjointement par Jonathan Boucher, postdoctorant dans le laboratoire de Philippe Roux, et Sherif Samer Attalla, étudiant au doctorat dans le laboratoire Muller.
![]()
-
28 June 2023 Concours de recrutement étudiant 2023 : une édition sous le signe des rencontres
L’édition 2023 s’est déroulée du 7 au 9 juin et a accueilli 23 participants et participantes provenant de 19 universités à travers le monde. Plus de cent entrevues ont été planifiées cette année entre les participants et participantes et les 12 chercheuses et chercheurs de l’Institut présents à l’événement.
![]()
-
28 June 2023 Les piliers de l’IRIC : rencontrez Isabelle Caron
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Isabelle Caron, technicienne en santé animale pour la plateforme de Biologie in vivo.
![]()
-
15 June 2023 Un Prix du recteur remis à Julie Mantovani pour le projet des Pauses connexion
Les Prix du recteur 2023 de l’Université de Montréal ont été remis le 12 juin pour célébrer les réalisations et l’engagement de membres du personnel qui se démarquent et illustrent de manière exceptionnelle les valeurs universitaires. L’IRIC félicite Julie Mantovani, cheffe des affaires académiques, qui a reçu le prix Innovation lors de la cérémonie. Ce prix célèbre une personne qui ose le changement en proposant et en mettant en œuvre de nouvelles idées.
![]()
-
13 June 2023 Les piliers de l’IRIC : rencontrez Raphaëlle Lambert
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Raphaëlle Lambert, responsable de la plateforme de génomique de l’IRIC.
![]()
-
5 June 2023 Le concours Science Réflexion de l’IRIC : de retour pour l’édition 2023 dès le 6 juin !
Nous avons le plaisir de vous annoncer le retour du concours Science Réflexion de l’IRIC!
Vous possédez une belle image de microscopie, une figure provenant de vos analyses bioinformatiques ou toute autre illustration issue de vos recherches?
Participez au concours et tentez de remporter une des 4 des cartes-cadeaux d’une valeur de 100$.
Les œuvres sélectionnées seront imprimées (par exemple en format 3’x3′) et disposées à des endroits stratégiques dans l’Institut. Les mêmes œuvres pourraient être offertes aux commanditaires dans le cadre d’activités philanthropiques.
![]()
-
2 June 2023 Les récipiendaires des bourses IRIC scientifiques de demain 2023 arrivent à l’Institut
Ce concours de bourses permet à des étudiants et étudiantes de premier cycle de venir effectuer un stage de recherche de 12 à 16 semaines à l’IRIC pendant le trimestre d’été.
![]()
-
2 June 2023 Un prix du public pour Juliette Humeau lors de la finale provinciale de Science POP
La finale provinciale du concours de communication scientifique Science POP s’est tenue les 27 et 28 mai derniers. Dans la catégorie vulgarisation, Juliette Humeau, postdoctorante dans le laboratoire de Claude Perreault, a remporté le prix du public pour sa présentation « L’action coordonnée des cellules immunitaires dans la lutte anticancéreuse ».
![]()
-
31 May 2023 Nomination de Philippe Roux au poste de directeur scientifique de l’IRIC
L’IRIC est heureux d’annoncer la nomination du professeur Philippe Roux au poste de directeur scientifique de l’Institut pour un mandat de deux ans. Le Conseil de l’Université de Montréal a récemment entériné la recommandation du conseil d’administration de l’IRIC. Le professeur Roux devient ainsi le troisième directeur scientifique de l’histoire de l’Institut, qui souligne ses 20 ans d’existence en 2023. Il succède à ce poste au professeur Marc Therrien, qui assumait cette fonction avec brio depuis 2013.
![]()
-
31 May 2023 La relève à l’honneur lors de la Journée scientifique de l’IRIC 2023
La 10e Journée scientifique de l’IRIC, tenue le 26 mai dernier, a permis de mettre en lumière le travail de la communauté scientifique de l’Institut. Plus de 150 personnes ont participé à l’événement qui comptait 12 présentations orales et 63 présentations par affiche au programme. Celles-ci ont suscité discussions et échanges dynamiques, qui pourront nourrir les réflexions de tous et toutes
![]()
-
30 May 2023 Les piliers de l’IRIC : rencontrez Caroline Baril
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Caroline Baril, agente de recherche dans le laboratoire de Marc Therrien à l’IRIC.
![]()
-
26 May 2023 Fondation de Richard et Edith Strauss : un soutien renouvelé de 300 000$!
Depuis 2019, grâce au généreux soutien de la Fondation de Richard et Edith Strauss, les chercheurs, les chercheuses et leurs équipes peuvent approfondir les recherches sur la leucémie pédiatrique et la leucémie aiguë myéloïde (LMA) et ainsi repousser les limites de la science sur ces types de cancer.
![]()
-
26 May 2023 Renouvellement du mandat de Michel Bouvier au poste de directeur général de l’IRIC
À l’issue de la 0178e séance tenue le 11 avril 2023, le Comité exécutif de l’Université de Montréal a nommé Michel Bouvier à titre de directeur général exécutif de l’Institut de recherche en immunologie et en cancérologie (IRIC) et ce, pour un quatrième mandat qui débutera le 1er juin 2023 et se terminera le 31 mai 2024.
![]()
-
25 May 2023 Une subvention NOVA pour Delphine Bouilly et ses partenaires
L’IRIC félicite Delphine Bouilly, directrice de l’Unité de recherche en conception et application de nanobiocapteurs électroniques, qui a obtenu une subvention NOVA de 225 000 $ sur trois ans pour le projet « Dispositifs de graphène bicouche fonctionnalisés : atteindre sélectivité et sensibilité ». Offerte conjointement par les Fonds de recherche du Québec – Nature et technologies et le Conseil de recherches en sciences naturelles et en génie du Canada, cette subvention soutient des projets de recherche dirigés par des chercheurs ou chercheuses de la relève du Québec en collaboration avec des chercheurs ou chercheuses des autres provinces canadiennes et territoires.
![]()
-
17 May 2023 La chercheuse Geneviève Deblois obtient un Prix Forbeck !
Geneviève Deblois, directrice de l’Unité de recherche sur les mécanismes épigénétiques et métabolisme du cancer de l’IRIC, fait partie des 13 récipiendaires du Prix Forbeck 2022-2023. « Ce prix me permettra de faire partie d’un groupe de chercheuses et chercheurs spécialisés, dont plusieurs reconnus mondialement dans des domaines de recherches connexes au mien. », explique Geneviève Deblois.
![]()
-
17 May 2023 Identification de Supervilline comme cible de ERK3 : des implications pour la complétion de la cytocinèse
Malgré des rôles potentiels dans la tumorigenèse des cellules de cancer du poumon et du sein, la protéine kinase atypique ERK3, membre de la voie Ras/MAPK, n’est que très peu caractérisée. Le laboratoire du professeur Sylvain Meloche, directeur de l’Unité de recherche en signalisation et croissance cellulaire, a collaboré avec le laboratoire du professeur Jean-Claude Labbé, directeur de l’Unité de recherche en division et différenciation cellulaire, tous deux à l’IRIC, pour identifier les cibles de ERK3 et mieux comprendre ses fonctions cellulaires. Les travaux menés ont permis d’identifier la protéine Supervilline comme étant une cible de ERK3. Publiée dans le Journal of Cellular Physiology, l’étude a été menée conjointement par le postdoctorant Joaquim Javary et la conseillère à la recherche Eugénie Goupil, avec la collaboration de la conseillère à la recherche Mathilde Soulez.
![]()
-
5 May 2023 Treize membres de l’IRIC sont récipiendaires de bourses et subventions des Fonds de recherche du Québec pour l’année 2023-2024
Les Fonds de recherche du Québec (FRQ) offrent 58,6 M$ en bourses de formation, 13,1 M$ en bourses de carrière et 29,8 M$ en subventions de recherche pour un total de 101,5 M$ en nouveaux octrois pour l’année 2023-2024. L’IRIC est fier de compter plusieurs de ses membres parmi les lauréats et lauréates de ces concours.
![]()
-
5 May 2023 Trois finalistes représenteront l’IRIC lors de la finale provinciale de Science Pop
Tenue le 12 avril dernier, la compétition interne de l’IRIC a couronné trois finalistes qui prendront part à la finale provinciale du concours panquébécois de communication scientifique Science Pop, les 27 et 28 mai prochains.
![]()
-
4 May 2023 Les piliers de l’IRIC: rencontrez Éric Bonneil
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Éric Bonneil, responsable de la plateforme de protéomique de l’IRIC.
![]()
-
4 May 2023 Soirée-bénéfice de l’IRIC : 505 000 $ amassés pour Audace 2023
Le 27 avril dernier, plus de 250 convives se sont réunis à l’occasion du 20e anniversaire de l’IRIC lors de son événement-bénéfice Audace. Grâce à la générosité des invités et des donateurs, plus de 505 000 $ ont été amassés afin de pérenniser la mission de l’IRIC et améliorer les thérapies contre le cancer.
![]()
-
4 May 2023 L’Université de Montpellier décerne un doctorat honorifique à Michel Bouvier
Un doctorat honoris causa a été remis à Michel Bouvier pour ses travaux sur les récepteurs couplés aux protéines G (RCPG) et sa contribution aux avancées scientifiques dans le domaine de la pharmacologie moléculaire. La plus haute distinction de l’enseignement supérieur lui a été décernée par l’Université de Montpellier au cours d’une cérémonie qui s’est tenue le 13 avril dernier.
![]()
-
2 May 2023 Félicitations aux récipiendaires des Bourses de congrès de l’IRIC - Compétition Hiver 2023
L’objectif du concours est de favoriser la participation des étudiants à la maîtrise, au doctorat et des stagiaires postdoctoraux de l’IRIC à des congrès scientifiques de grande envergure qui se déroulent hors de la province du Québec.
![]()
-
4 April 2023 Découverte de nouveaux rôles pour eIF4E : reprogrammation de masse de l’épissage pour changer le message
L’équipe de la professeure Katherine Borden, directrice de l’Unité en structure et fonction du noyau cellulaire de l’IRIC, a voulu comprendre comment l’épissage alternatif était détourné chez certaines personnes atteintes de la leucémie myéloïde aiguë (LMA) qui ne présentent pas les mutations de l’ADN habituellement impliquées dans ce détournement. L’étude de modèles de laboratoires et d’échantillons de personnes leucémiques a permis de découvrir que l’épissage de milliers d’ARNs pouvait être altéré de façon insoupçonnée par la protéine oncogène eIF4E, conférant des propriétés cancéreuses aux cellules. Publié dans le journal EMBO, le travail a été mené conjointement par les postdoctorants Mehdi Ghram et Gavin Morris, ainsi que par l’associée de recherche Biljana Culjkovic-Kraljacic.
![]()
-
14 March 2023 Plus de 10 000$ amassés pour la première édition de FOCUS!
Du 9 février au 12 février 2023 avait lieu la première édition de FOCUS, une exposition présentant la science sous un angle artistique grâce au talent créatif de la communauté scientifique de l’IRIC. L’exposition a mis en lumière des œuvres scientifiques créées par la communauté de l’Institut à Projet Casa, une salle d’exposition montréalaise fondée par des mécènes de longue date de l’IRIC : Danielle Lysaught et Paul Hamelin.
![Focus]()
-
14 March 2023 Les piliers de l’IRIC: rencontrez Nadine Mayotte
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu.
Aujourd’hui, rencontrez Nadine Mayotte, conseillère à la recherche dans le laboratoire de Guy Sauvageau à l’IRIC.
![]()
-
14 March 2023 Le chercheur Gregory Emery obtient une subvention des Instituts de recherche en santé du Canada
Le concours de subventions Projet des Instituts de recherche en santé du Canada (IRSC) vise à soutenir les idées originales ayant le potentiel de faire avancer les connaissances fondamentales et appliquées en santé. La plus récente édition du concours, tenue à l’automne 2022, a financé 382 demandes, pour un investissement total de 325 millions de dollars. L’IRIC tient à féliciter Gregory Emery, directeur de son Unité de recherche en transport vésiculaire et signalisation cellulaire, qui est du nombre. Une subvention de 963 900 $ sur cinq ans lui a été octroyée pour le projet « Régulation de la migration cellulaire collective par la kinase Misshapen ».
![]()
-
8 March 2023 Le chercheur David Knapp obtient une subvention de l’Institut de recherche Terry Fox
David Knapp, directeur de l’Unité de recherche en ingénierie cellulaire de l’IRIC, fait partie des récipiendaires 2023 des Terry Fox New Investigator Awards. Il recevra 433 850 $ sur trois ans pour le projet « Compréhension des mécanismes moléculaires de l’hématopoïèse clonale associée à l’âge ».
![]()
-
8 March 2023 Signature d’un accord de licence exclusif et d’une nouvelle collaboration de recherche en oncologie avec la compagnie Ipsen
L’Institut de recherche en immunologie et en cancérologie de l’Université de Montréal, l’IRIC, est fier d’annoncer que la compagnie Ipsen a exercé son option de licence pour l’acquisition des droits exclusifs d’un de ses programmes de recherche pré-clinique en oncologie, résultat d’une collaboration de recherche fructueuse entre Ipsen, IRICoR, et l’Université de Montréal, initiée en mai 2020. Ipsen mènera désormais l’ensemble des activités de développement et de commercialisation de ce candidat-médicament à l’échelle mondiale.
![]()
-
7 March 2023 Bourses de maîtrise et de doctorat de l’IRIC – Récipiendaires du Concours Automne 2022
L’objectif du Concours Bourses de maîtrise et de doctorat de l’IRIC 2022-2023 est d’appuyer les étudiantes et étudiants de l’IRIC qui ont un excellent dossier académique et de recherche, mais qui ne bénéficient pas de bourse nominale majeure. Les bourses de maîtrise et doctorat sont offertes grâce à l’appui de la grande communauté de l’IRIC : ses employées et employés, ses chercheuses et chercheurs et ses généreuses et généreux donateurs et partenaires. L’octroi de ces bourses est également rendu possible grâce à l’implication de plusieurs bénévoles.
![]()
-
16 February 2023 L’IRIC adopte de nouvelles lignes directrices pour les versements des bourses de maîtrise et de doctorat
Dans le contexte inflationniste actuel, l’IRIC a adopté en janvier 2023 de nouvelles mesures pour améliorer les conditions de vie et de travail de sa communauté étudiante. Le coût de la vie ayant augmenté en deux décennies, et particulièrement au cours des deux dernières années, les nouvelles lignes directrices adoptées par l’IRIC permettront de réduire le stress financier de sa communauté étudiante et de fournir un climat plus sain pour réaliser des études.
![]()
-
13 February 2023 Les piliers de l’IRIC: rencontrez Gabrielle Jacob
En 2023, l’IRIC fête ses 20 ans. Parmi les initiatives mises en place pour célébrer cet anniversaire, la série de portraits « Les piliers de l’IRIC » permettra de mettre en lumière les personnes qui ont contribué depuis les tous débuts, parfois dans l’ombre, à faire de l’IRIC ce qu’il est devenu. Aujourd’hui, rencontrez Gabrielle Jacob, technicienne en administration au sein de l’équipe des finances de l’IRIC.
![]()
-
6 February 2023 Un soutien renouvelé au Fonds Valérie Blais
Un soutien renouvelé au Fonds Valérie Blais
![]()
-
2 February 2023 L’IRIC et ses partenaires se rencontrent à Montpellier pour développer un programme de maîtrise internationale
Fruit d’une collaboration entre l’IRIC, l’Université de Montréal, l’Université de Montpellier en France et l’Université de Pavie en Italie, le projet « MAD4Cancer – Towards an International Master Degree in Cancer Biology » a obtenu un financement Erasmus Mondus Design Measures de 55 000 euros pour 15 mois. L’objectif du projet est de mettre sur pied un programme de maîtrise international en biologie du cancer permettant aux étudiantes et étudiants de fréquenter les trois universités partenaires.
![]()
-
27 January 2023 La Fondation Jean Gaulin fait un don de 24 420$ au Fonds général de l’IRIC
La fondation familiale privée de Jean Gaulin a comme mission de soutenir le bien-être de la communauté. Depuis plusieurs années, la fondation appuie l’Institut et veille à approfondir les connaissances en immunologie et en cancérologie. Ce don contribua à convertir les découvertes des chercheurs et chercheuses en solutions thérapeutiques novatrices pour le bien-être des personnes touchées par le cancer.
![]()
-
20 January 2023 Nomination de William Brock à titre de président du conseil d’administration de l’IRIC
L’IRIC annonce avec enthousiasme la nomination de Me William Brock, avocat émérite du Barreau du Québec, à titre de nouveau président du CA.
![]()
-
7 December 2022 L’utilisation du marqueur CAXII pourrait améliorer la classification des tumeurs mammaires
Le cancer du sein est une maladie hétérogène, qui ne peut être ciblée efficacement par un traitement commun et unique. Dans deux tiers des cas, le récepteur des œstrogènes de type alpha (ERα), un récepteur activé par les hormones sexuelles, est exprimé et peut être ciblé thérapeutiquement par une hormonothérapie. Toutefois, les niveaux d’ERα peuvent varier d’une tumeur à l’autre et à l’intérieur même des tumeurs, compliquant sa détection et le choix subséquent de la thérapie. Le récepteur de la progestérone (PR) est couramment utilisé en clinique comme co-marqueur de sélection de tumeurs se qualifiant pour une hormonothérapie. En effet, ce marqueur régulé par les œstrogènes est censé refléter l’activité d’ERa. Dans une nouvelle étude parue dans le journal Cancers, Sylvie Mader, directrice de l’Unité de recherche en ciblage moléculaire dans le traitement du cancer du sein de l’IRIC, et son étudiant au doctorat Lucas Porras montrent que la détection de PR reflète imparfaitement l’activité d’ERα et identifient un nouveau co-marqueur plus fiable.
![]()
-
28 November 2022 Une greffe de moelle osseuse unit Dr Claude Perreault et Dr Robert Patenaude depuis maintenant 40 ans
Novembre 2022 marque le 40e anniversaire d’une rencontre clé ayant permis à Robert Patenaude de devenir l’un des premiers bénéficiaires d’une greffe de moelle osseuse au pays. Retour sur cette histoire unissant solidement Robert Patenaude à Claude Perreault depuis maintenant quatre décennies.
![]()
-
24 November 2022 Identification de CDK12 comme nouvelle cible de la voie RAS/MAPK : des implications pour le traitement des mélanomes
Le laboratoire du professeur Philippe P. Roux, directeur de l’Unité de recherche en signalisation cellulaire et protéomique, s’est intéressé aux mécanismes associés à cette résistance. Pour découvrir des cibles anti-cancéreuses plus efficaces, l’équipe a cherché à identifier les effecteurs clés de la voie RAS/MAPK, une voie de signalisation suractivée dans les mélanomes. Les travaux effectués ont permis d’identifier la protéine CDK12 comme étant une cible directe de la voie et de mettre en lumière son rôle important dans les cellules de mélanome. Le projet a été mené par le postdoctorant Thibault Houles et fait l’objet d’une publication dans le journal Nature Communications.
![]()
-
21 November 2022 Brian Wilhelm et ses partenaires reçoivent plus de 2 millions de dollars pour un projet de recherche sur les leucémies pédiatriques
Un partenariat inédit rassemblant le Conseil québécois sur la découverte du médicament (CQDM), la Société canadienne du cancer (SCC), la Fondation Cole, l’Oncopole, des philanthropes et des entreprises québécoises a permis de remettre 8 485 132 $ à quatre équipes montréalaises pour leurs projets de recherche sur les cancers pédiatriques. Parmi ces dernières se trouve l’équipe de Brian Wilhelm, directeur de l’Unité de recherche en génomique à haut débit à l’IRIC et professeur agrégé au Département de médecine de la Faculté de médecine de l’Université de Montréal.
![]()
-
25 October 2022 Objectifs atteints pour les événements sportifs au bénéfice de l’IRIC
Cet automne, notre communauté a eu l’occasion de se joindre à trois initiatives sportives de renom en participant à différentes compétitions et / ou en soutenant la cause de l’IRIC. Au total, une somme de 21 325 $ a pu être remise à l’Institut grâce à la générosité et à la détermination de nos amatrices et amateurs de sports! Retour sur ces événements.
![]()
-
24 October 2022 Un jeune chercheur qui a le vent dans les voiles
David Knapp, directeur de l’Unité de recherche en ingénierie cellulaire de l’IRIC et professeur adjoint au Département de pathologie et biologie cellulaire de la Faculté de médecine de l’Université de Montréal, cumule les bons coups, deux ans seulement après l’établissement de son groupe de recherche. Faisant partie des plus récents récipiendaires du concours annuel de subventions de la Société de recherche sur le cancer, David Knapp et son équipe ont également collaboré à deux études publiées cet été. Retour sur ces accomplissements.
![]()
-
21 October 2022 La postdoctorante Juliette Humeau obtient une bourse salariale
Dans le cadre de son plus récent Concours de bourses salariales de l’IRIC, tenu cet automne, l’IRIC a remis une bourse postdoctorale grâce au fonds Power Corporation Canada de la relève scientifique. Juliette Humeau, postdoctorante dans le laboratoire de Claude Perreault, s’est vue octroyée ce financement en raison de la qualité de son dossier académique et scientifique.
![]()
-
13 October 2022 Les Grandes Retrouvailles à l’IRIC : quand les portes des laboratoires s’ouvrent pour le grand public
L’Université de Montréal a tenu ses premières Grandes Retrouvailles sur ses différents campus, du 28 septembre au 2 octobre derniers. Dans le cadre de l’événement, qui comptait une cinquantaine d’activités, 17 personnes ont pu visiter les installations de l’IRIC et découvrir son modèle de recherche en cancérologie.
![]()
-
11 October 2022 Une percée majeure née d’une collaboration internationale ouvre le chemin vers le soulagement de la douleur
Le projet est le fruit d’une collaboration internationale entre des groupes de recherche de différents domaines : Brian Shoichet et Allan Basbaum, tous deux chercheurs à l’University of California San Francisco, Peter Gmeiner de l’Université Freidrichs Alexander en Allemagne, Yang Du de l’Université chinoise de Hong Kong et Michel Bouvier, directeur général de l’IRIC et directeur de l’Unité de recherche en pharmacologie moléculaire. Ces travaux font l’objet d’une publication dans le journal Science.
![]()
-
3 October 2022 Deux projets de l’IRIC retenus lors du plus récent concours annuel de la Société de recherche sur le cancer
La Société de recherche sur le cancer (SRC) a dévoilé les récipiendaires des 90 nouvelles subventions de recherche octroyées lors de son plus récent concours annuel. Deux équipes de l’IRIC en font partie.
![]()
-
23 September 2022 Deux nouveaux récipiendaires se méritent une Bourse postdoctorale Power Corporation du Canada de la relève scientifique
À l’issue du concours de Bourses postdoctorales Power Corporation du Canada de la relève scientifique, tenu cet été, deux postdoctorants de l’IRIC se méritent un financement grâce à la qualité de leurs travaux de recherche.
![]()
-
16 September 2022 Quatre étudiantes et étudiants de l’IRIC obtiennent du financement pour aller présenter leurs résultats de recherche hors Québec
Dans le cadre de son plus récent concours de Bourses de congrès, l’IRIC a remis des bourses à quatre doctorantes et doctorants. Ce soutien financier leur permettra de présenter leurs résultats de recherche lors de congrès scientifiques tenus en dehors du Québec.
![]()
-
12 September 2022 L’engagement exceptionnel de la Katelyn Bedard Bone Marrow Association
L’IRIC désire mettre en lumière le soutien exemplaire de la Katelyn Bedard Bone Marrow Association qui appuie depuis 15 ans les travaux de l’équipe du Dr Claude Perreault. En 2022, un don de 10 000 $ a été acheminé et à ce jour, c’est un montant de 90 000 $ qui a été versé au laboratoire Perreault pour propulser la recherche sur la transplantation de cellules hématopoïétiques et le traitement des leucémies.
![]()
-
9 September 2022 IRIC sur la route : l’équipe des affaires académiques entreprend une tournée de recrutement
Dans le cadre de sa tournée de recrutement étudiant IRIC sur la route, l’équipe des affaires académiques de l’Institut participera cet automne à plusieurs salons d’études supérieures organisés par des universités canadiennes.
![]()
-
7 September 2022 Katherine Borden est élue à la Société royale du Canada
La professeur Katherine Borden, directrice de l’Unité de recherche en structure et fonction du noyau cellulaire de l’IRIC et professeure titulaire au Département de pathologie et biologie cellulaire de la Faculté de médecine de l’Université de Montréal, a été élue membre de l’Académie des sciences de la Société royale du Canada (SRC).
![]()
-
22 August 2022 Une molécule chimique conçue à l’IRIC a été nommée « molécule du mois » en juin 2022 par la plateforme Drug Hunter
Candidat clinique conçu et synthétisé à l’IRIC par l’Unité de Découverte du Médicament dirigée par la chercheuse principale Anne Marinier, la molécule BMS-986120 (UDM-002985) a été nommée « molécule du mois » par la plateforme Drug Hunter.
![]()
-
11 August 2022 La Journée des stagiaires d’été de l’IRIC : une belle expérience pour apprendre à communiquer ses résultats de recherche
La quatrième édition de la Journée des stagiaires d’été de l’IRIC s’est tenue le jeudi 11 août 2022. L’événement, organisé par le Bureau des affaires académiques de l’IRIC de pair avec les stagiaires d’été, a permis à 10 stagiaires de s’initier à la communication scientifique.
![]()
-
21 July 2022 Découverte d’une nouvelle avenue thérapeutique ciblant le cycle cellulaire dans un sous-type de leucémie myéloïde aiguë
Le projet, mené par l’agente de recherche Céline Moison, fait l’objet d’une publication dans le journal Blood Advances. Le travail a été réalisé grâce à la collaboration des équipes de Guy Sauvageau et Anne Marinier à l’IRIC, Josée Hébert de l’Hôpital Maisonneuve-Rosemont et Vincent-Philippe Lavallée du CHU Sainte-Justine.
![]()
-
19 July 2022 Quatre chercheurs de l’IRIC obtiennent du financement des Instituts de recherche en santé du Canada
À l’issue du plus récent concours de subventions de recherche des Instituts de recherche en santé du Canada (IRSC), quatre chercheurs de l’IRIC obtiennent des fonds du programme de subvention Projet.
![]()
-
8 July 2022 Cinq finissantes et finissants de l’IRIC nominés à la liste d’honneur du Recteur de l’Université de Montréal
L’IRIC est fier de compter cinq de ses finissants et finissantes parmi les plus récentes nominations à la liste d’honneur du Recteur.
![]()
-
5 July 2022 Trois chercheurs de l’IRIC reçoivent des fonds du Conseil des recherches en sciences naturelles et en génie du Canada
Le Conseil des recherches en sciences naturelles et en génie du Canada (CRSNG) a récemment dévoilé les résultats de son concours de subvention de recherche 2022. Plus de 430 millions de dollars seront remis à des chercheurs et chercheuses de partout au pays afin de mener à bien leurs programmes de recherche. À l’issue du concours 2022, trois chercheurs de l’IRIC se sont vus octroyer des subventions.
![]()
-
29 June 2022 L’IRIC recrute le Dr Vincent Q. Trinh à titre de chercheur principal
L’Institut de recherche en immunologie et en cancérologie (IRIC) de l’Université de Montréal est fier de souligner l’arrivée en ses murs d’un nouveau chercheur principal à l’Unité de recherche en histologie digitale et pathologie avancée, le Dr Vincent Q. Trinh, lequel entrera en fonction le 1er juillet 2022.
![]()
-
29 June 2022 Rencontrez Vincent Q. Trinh, nouveau chercheur à l’IRIC
L’Institut de recherche en immunologie et en cancérologie (IRIC) de l’Université de Montréal est fier de souligner l’arrivée en ses murs d’un nouveau chercheur principal à l’Unité de recherche en histologie digitale et pathologie avancée, le Dr Vincent Q. Trinh, lequel entrera en fonction le 1er juillet 2022. Dr Trinh a accepté avec enthousiasme de répondre à quelques questions.
![]()
-
27 June 2022 Hyperactivation de la voie NOTCH1 dans la leucémie aiguë lymphoblastique à cellules T : deux publications récentes apportent un nouvel éclairage
L’équipe de Trang Hoang, directrice de l’unité de recherche en hématopoïèse et leucémie de l’IRIC, s’est intéressée à l’hyperactivation de NOTCH1 dans la T-ALL. Le travail de Diogo Veiga, postdoctorant désormais professeur de génomique et bio-informatique à l’Universidade Estadual de Campinas au Brésil, et Mathieu Tremblay, conseiller à la recherche, a permis la publication de deux articles.
![]()
-
22 June 2022 Michel Bouvier nommé Chevalier de l’Ordre national du Québec
Le 22 juin 2022, Michel Bouvier, directeur général de l’IRIC, chercheur principal de l’Unité de recherche en pharmacologie moléculaire et Professeur au Département de biochimie et médecine moléculaire de la Faculté de médecine de l’Université de Montréal est nommé Chevalier de l’Ordre national du Québec.
![]()
-
21 June 2022 Bourses IRIC scientifiques de demain 2022: douze stagiaires travailleront à l’IRIC cet été
Douze étudiantes et étudiants ont l’opportunité de compléter un stage de recherche de 12 ou de 16 semaines à l’IRIC, en plus de bénéficier d’une bourse d’excellence d’un montant de 4 800$ ou de 6400$ respectivement.
![]()
-
21 June 2022 Retour en présentiel pour l’édition 2022 du Concours de recrutement étudiant de l’IRIC
L’édition 2022 du concours s’est déroulée du 1 au 3 juin et a accueilli 29 participants et participantes provenant de 18 universités à travers le monde. Cent-cinquante-trois entrevues ont été planifiées cette année entre les participants et participantes et les 14 chercheuses et chercheurs de l’Institut présents à l’événement.
![]()
-
8 June 2022 Neuf scientifiques de la relève de l’IRIC reçoivent une bourse de formation des Fonds de recherche du Québec
À l’issue des concours 2022-2023, les Fonds de recherche du Québec (FRQ) ont remis 39,3M$ en bourses de formation. L’IRIC est fier de compter neuf scientifiques de sa relève parmi les lauréats et lauréates des concours.
![]()
-
26 May 2022 Claude Perreault et Pierre Thibault, fondateurs d’Epitopea, une compagnie porteuse d’espoir pour le traitement du cancer
Fondée en 2021, la société de biotechnologie transatlantique Epitopea voit le jour à la suite de collaborations entre les équipes de Claude Perreault et de Pierre Thibault, tous deux chercheurs principaux à l’IRIC. L’organisation a pour mission de développer des immunothérapies pour traiter les différents types de cancers en ciblant une nouvelle classe d’antigènes.
![]()
-
20 May 2022 Un soutien de 3 millions de dollars du Réseau de cellules souches pour étudier de nouvelles façons d’utiliser les cellules souches sanguines dans le traitement des leucémies
Guy Sauvageau, chercheur principal à l’IRIC, hématologue et professeur titulaire au Département de médecine de la Faculté de médecine de l’Université de Montréal, est récipiendaire d’un financement majeur d’une valeur de 3 millions de dollars sur trois ans. Le projet mené par Dr Sauvageau est composé de 8 groupes de recherche dont ceux de Philippe Roux et d’Étienne Gagnon, tous deux chercheurs à l’IRIC.
![]()
-
16 May 2022 Vincent Archambault nommé professeur titulaire au Département de biochimie et médecine moléculaire de l’Université de Montréal
L’IRIC est fier d’annoncer la promotion de Vincent Archambault, chercheur principal et directeur de l’unité de recherche sur la régulation du cycle cellulaire, comme professeur titulaire au Département de biochimie et médecine moléculaire de l’Université de Montréal.
![]()
-
12 May 2022 Les Rendez-vous Audace 2022 : la Dre Eralda Kina répond à vos questions
Les Rendez-vous Audace de l’IRIC, tenus le 27 avril dernier, ont rassemblé André Robitaille et trois interlocutrices inspirantes autour du thème « Un monde en transformation, une relève en action ». Eralda Kina, oncologue et doctorante à l’IRIC dans le laboratoire de Claude Perreault, a quant à elle discuté de son expérience de clinicienne et des grands espoirs qu’elle fonde en la recherche en immunologie et en cancérologie. Dre Kina a généreusement accepté de répondre aux questions du public reçues lors de la diffusion des Rendez-vous Audace.
![]()
-
9 May 2022 Geneviève Deblois est honorée par les Instituts de recherche en santé du Canada
Geneviève Deblois, chercheuse principale à l’IRIC et professeure adjointe à la Faculté de pharmacie de l’Université de Montréal, est lauréate du Prix de début de carrière en recherche sur le cancer 2022. Ce prix, remis par l’Institut du cancer des Instituts de recherche en santé du Canada (IRSC), reconnaît l’excellence de la recherche réalisée au Canada. Il est remis aux nouveaux chercheurs et chercheuses ayant présenté les demandes de subventions les mieux classées du concours d’automne des IRSC, volet Projet.
![]()
-
28 April 2022 Identification d’un nouveau rôle clé pour les microtubules interphasiques en entrée de mitose
Au début de la division cellulaire, les cellules s’arrondissent entre autres via la réorganisation de leur cortex. Parmi les protéines impliquées dans cette morphogenèse, on trouve la famille des protéines ERM (ezrine, radixine et moésine). L’équipe du professeur Sébastien Carréno, directeur de l’unité de recherche sur les mécanismes de la morphogénèse cellulaire au cours de la mitose et de la migration, a voulu identifier le signal d’activation de ces protéines en entrée de mitose. Leurs travaux ont mis en lumière un nouveau mécanisme impliquant les microtubules interphasiques dans la régulation de l’arrondissement cellulaire en entrée de mitose. Le projet, mené par l’étudiant au doctorat Kévin Leguay, fait l’objet d’une publication dans le Journal of Cell Biology.
![]()
-
20 April 2022 Nouvelle entente de collaboration internationale de recherche en découverte de médicaments
L’IRIC se réjouit de la signature d’un accord de collaboration entre Ono Pharmaceutical Co., Ltd., une des plus grandes sociétés pharmaceutiques de stade clinique du Japon, Domain Therapeutics S.A. et l’Université de Montréal, qui vise à découvrir de nouvelles petites molécules ciblant les récepteurs couplés aux protéines G (RCPG) dans le traitement de maladies métaboliques.
![]()
-
12 April 2022 Publication de deux études caractérisant la sélectivité de couplage des récepteurs couplés aux protéines G
Les deux tiers des hormones humaines ainsi que le tiers des médicaments ciblent et activent la famille des récepteurs couplés aux protéines G (RCPG). Pour un même récepteur, différents ligands peuvent engager sélectivement différents sous-ensembles de voies de signalisation. La cartographie des effecteurs pouvant être engagés par un récepteur donné est essentielle pour comprendre les processus physiologiques de même que pour concevoir des médicaments plus sûrs. L’équipe du professeur Michel Bouvier, directeur de l’unité de recherche en pharmacologie moléculaire et directeur général de l’IRIC, s’est penchée sur la caractérisation de la sélectivité de couplage des RCPG.
![]()
-
7 March 2022 L’IRIC célèbre la Journée internationale des femmes
L’IRIC profite de la Journée internationale des droits des femmes pour reconnaître et souligner la contribution exceptionnelle de toutes ses scientifiques qui travaillent à faire la différence.
![]()
-
23 February 2022 Doctorante à l’IRIC, Assya Trofimov est lauréate de la prestigieuse bourse postdoctorale Mahan
Assya Trofimov, étudiante au doctorat en co-direction dans les laboratoires de Claude Perreault et de Sébastien Lemieux, a obtenu la prestigieuse bourse postdoctorale Mahan. Le concours, tenu annuellement par le Fred Hutchison Cancer Research Center (Fred Hutch) de Seattle, récompense les candidatures exceptionnelles en offrant un support financier de 21 mois pour réaliser un projet de recherche dans un de ses laboratoires de biologie computationnelle.
![]()
-
17 February 2022 Trois événements sportifs au profit de l’IRIC
En 2022, la communauté de l’IRIC aura l’occasion de participer à trois événements sportifs de renom : Les Défis du Parc national de la Mauricie, Les Grands Prix Cyclistes de Québec et de Montréal, ainsi que le Marathon Beneva de Montréal.
![]()
-
11 February 2022 L’IRIC souligne la Journée internationale 2022 des femmes et des filles de science
À l’occasion de cette journée symbolique, l’IRIC est fier de souligner la contribution exceptionnelle de toutes ses membres dans la recherche contre le cancer.
![]()
-
4 February 2022 Quatre laboratoires de l’IRIC reçoivent une subvention des Instituts de recherche en santé du Canada
Lors du concours d’automne 2021, quatre équipes de recherche de l’IRIC se sont vues octroyer des prestigieuses subventions.
![]()
-
4 February 2022 La leçon d’une vie du marathonien Jean Mireault
En cette Journée mondiale contre le cancer, l’IRIC désire souligner la généreuse contribution de monsieur Jean Mireault envers notre cause. Le 11 octobre 2021, monsieur Mireault a participé au marathon de Boston en l’honneur de sa mère décédée très jeune des suites du cancer. Bien que sa course ne se soit pas déroulée comme il l’espérait en raison d’un malaise inattendu à la mi-parcours, monsieur Mireault en retire une leçon des plus inspirantes pour chacun de nous. Dans un témoignage empreint de franchise, il nous raconte dans quel état d’esprit il a pu compléter, non pas sans heurt, la deuxième partie de son marathon.
![]()
-
28 January 2022 Renouvellement du mandat de Michel Bouvier au poste de directeur général de l’IRIC
À l’issue d’une séance du comité exécutif, tenu le 7 décembre 2021, l’Université de Montréal a annoncé la poursuite du mandat de Michel Bouvier au poste de directeur général de l’IRIC pour un troisième mandat d’un an.
![]()
-
27 January 2022 L’IRIC obtient un financement majeur pour élaborer une chimiothèque intelligente
Dans le cadre de la première phase de Médicament Québec, l’IRIC a récemment obtenu un financement majeur de 3 200 045 $ pour le projet Accroissement des capacités et de la qualité de chimiothèques pour la découverte de médicaments.
![]()
-
26 January 2022 Katherine Borden est honorée par la Société canadienne des biosciences moléculaires
La Société canadienne pour les biosciences moléculaires (SCBM) remet le prestigieux Prix du Scientifique chevronné de Canadian Science Publishing 2022 à Katherine Borden, chercheuse principale à l’IRIC et professeure titulaire au Département de pathologie et biologie cellulaire de la Faculté de médecine de l’Université de Montréal.
![]()
-
20 January 2022 Un important soutien des National Institutes of Health pour étudier de nouvelles façons de cibler la leucémie myéloïde aiguë
La professeure Katherine Borden, chercheuse principale qui dirige l’unité de recherche en structure et fonction du noyau cellulaire de l’IRIC, a reçu une subvention d’une valeur de 1,47 million de dollars américains (1,85 million de dollars canadiens) sur cinq ans. Le financement octroyé par les National Institutes of Health (NIH), principal organisme subventionnaire de la recherche biomédicale aux États-Unis, soutiendra son projet de recherche visant à élucider les mécanismes moléculaires de transformation tumorale médiée par la protéine eIF4E.
![]()
-
18 January 2022 Identification d’une nouvelle voie de signalisation oncogénique dans le développement du carcinome hépatocellulaire
Le carcinome hépatocellulaire (CHC) est le 6e cancer le plus fréquemment diagnostiqué, et arrive au troisième rang des cancers les plus meurtriers dans le monde. Malgré ces chiffres imposants, les quelques traitements disponibles actuellement n’ont que des effets modestes chez les personnes atteintes, qui sont souvent diagnostiquées à un stade tardif de la maladie. Une plus grande compréhension mécanistique du développement du CHC est requise pour le contrer plus efficacement par de nouvelles thérapies ciblées. L’équipe du professeur Sylvain Meloche, directeur de l’unité de recherche en signalisation et croissance cellulaire de l’IRIC, a récemment mis en lumière une voie de signalisation oncogénique précédemment inconnue pour le CHC. Jean-Philippe Guégan et Marjorie Lapouge sont les co-premiers auteurs de l’article publié en janvier dans le journal Science Signaling.
![]()
-
14 December 2021 Bourses de maîtrise et de doctorat de l’IRIC – Récipiendaires du Concours Automne 2021
À l’issue du Concours de bourses de maîtrise et de doctorat de l’IRIC tenu cet automne, l’Institut est fier d’annoncer les 14 récipiendaires de cette édition.
L’objectif du concours est d’appuyer les étudiantes et les étudiants de l’Institut qui ont un excellent dossier académique et de recherche, mais qui ne bénéficient pas de bourse nominale majeure.
Félicitations à toutes et à tous!
![]()
-
13 December 2021 L’IRIC, un acteur clé du projet Acuité-Québec: 27M$ pour accélérer la découverte de nouveaux médicaments
L’Institut de recherche en immunologie et en cancérologie (IRIC) de l’Université de Montréal se réjouit de faire partie du projet Acuité-Québec, une initiative visant à favoriser la découverte de nouveaux médicaments.
![]()
-
16 November 2021 Recrutement à la direction scientifique de l’IRIC
L’IRIC sollicite des candidatures pour le poste de directeur/directrice scientifique et de chercheur principal/chercheuse principale à l’institut. On recherche une ou un scientifique chevronné ayant une carrière exceptionnelle afin de superviser le développement scientifique de l’Institut tout en menant son propre programme en recherche fondamentale et/ou translationnelle dans des domaines liés au cancer.
![]()
-
15 November 2021 Organisez une collecte de fonds pour soutenir les efforts de recherche en cancérologie
En cette Journée de la philanthropie, l’IRIC met en ligne un nouvel outil pour tous ceux et celles désirant organiser une activité de collecte de fonds au profit de l’Institut.
![]()
-
30 September 2021 Trang Hoang remporte le prix Mentor scientifique 2021 du Club de Recherches Cliniques du Québec
Trang Hoang, chercheuse principale à l’Institut de Recherche en Immunologie et en Cancérologie (IRIC) et professeure titulaire au Département de pharmacologie de la Faculté de médecine de l’Université de Montréal, s’est vu décerner le prix Mentor scientifique 2021 du Club de Recherches Cliniques du Québec (CRCQ).
![]()
-
21 September 2021 Un forum pour la semaine de l’égalité des sexes au Canada
En tant qu’institution, l’IRIC cherche à promouvoir l’équité et à accroître la diversité et l’inclusion, sous toutes ses formes, dans ses différents programmes.
![]()
-
29 July 2021 L’équipe de Pierre Thibault partage ses connaissances sur les stratégies protéomiques basées sur la spectrométrie de masse utilisées pour étudier les modifications de type UBL
Le groupe de Pierre Thibault, chercheur principal à l’IRIC et professeur au Département de chimie de l’UdeM, avec un collègue du Centre médical universitaire de Leiden aux Pays-Bas, a récemment publié un article de synthèse exhaustif dans la revue Nature Reviews Methods Primers pour informer les chercheurs de tous niveaux sur la variété des stratégies protéomiques basées sur la spectrométrie de masse utilisées pour étudier les modifications de type ubiquitine (UBL) et décrire le genre de données pouvant être générées par ces approches.
![]()
-
21 June 2021 Brian Wilhelm est récipiendaire d’un financement majeur dans le cadre du nouveau Programme d’intégration de la génomique initié par Génome Québec
Brian Wilhelm, chercheur principal à l’IRIC et professeur agrégé au Département de médecine de la Faculté de médecine de l’Université de Montréal, est récipiendaire d’un financement majeur dans le cadre du nouveau Programme d’intégration de la génomique – volet santé humaine, initié par Génome Québec en collaboration avec l’Oncopole.
![]()
-
17 June 2021 L’IRIC félicite l’engagement du gouvernement du Québec : 13 M$ investis pour fédérer les acteurs en découverte et production de médicaments
L’IRIC se réjouit de la création de « Médicament Québec », un pôle stratégique d’importance ayant pour mission de favoriser une meilleure autonomie et d’accroître le dynamisme du Québec en matière de découverte, de développement ainsi que de production de médicaments.
![]()
-
3 June 2021 Nomination de Clarissa Desjardins et renouvellement des mandats de Jacques Bernier et de Robert Paré au sein du CA de l’IRIC
L’IRIC est heureux d’annoncer la nomination de Clarissa Desjardins à titre de nouveau membre du conseil d’administration ainsi que le renouvellement des mandats de M. Jacques Bernier et de M. Robert Paré comme membres du CA par le comité exécutif de l’Université de Montréal.
![]()
-
26 May 2021 L’IRIC participe au prochain Forum de la Chambre de commerce du Montréal métropolitain
Lundi, le 31 mai prochain, l’IRIC participera au Forum stratégique Universités, cégeps, entreprises : collaborer pour une économie forte, innovante et socialement responsable, une initiative de la Chambre de commerce du Montréal métropolitain et du FRQS.
![]()
-
17 May 2021 Trang Hoang est la lauréate du prix Jeanne Manery Fisher 2021 de la SCBM
Trang Hoang, chercheuse principale à l’Institut de recherche en immunologie et en cancérologie (IRIC) et professeure titulaire au Département de pharmacologie de la Faculté de médecine de l’Université de Montréal, est la lauréate du prix Jeanne Manery Fisher 2021 de la Société canadienne pour les biosciences moléculaires (SCBM).
![]()
-
14 May 2021 Les Rendez-vous Audace 2021 : 320 000 dollars amassés pour soutenir les efforts de recherche de l’IRIC en cancérologie
Exceptionnellement cette année, l’Institut de recherche en immunologie et en cancérologie (IRIC) de l’Université de Montréal a présenté une formule virtuelle de son traditionnel événement-bénéfice Audace : Les Rendez-vous Audace. Pour l’occasion, environ 615 personnes en provenance de 8 pays ont assisté aux trois conférences présentées gratuitement, et près d’une vingtaine de commanditaires ont soutenu l’événement. Grâce à la générosité de nos partenaires et donateurs, un montant de 320 000 $ a été amassé pour accélérer la découverte de meilleures thérapies au bénéfice des patients.
![]()
-
11 May 2021 Conférence de Roger D. Kornberg – Prix Nobel de chimie
Le 20 mai prochain, l’IRIC et l’Université de Montréal auront l’honneur d’accueillir Roger D. Kornberg, Prix Nobel de chimie en 2006, dans le cadre d’une conférence intitulée : « Chromosome Structure and Transcription ».
![]()
-
26 April 2021 Des criblages à l’échelle du génome identifient un nouveau gène qui atténue la réponse aux dommages à l’ADN dans les cellules humaines avec des télomères érodés
Les télomères sont des séquences d’ADN qui servent de capuchons structuraux pour protéger les extrémités des chromosomes contre la dégradation, l’effilochage et la fusion avec d’autres chromosomes. Ils jouent un rôle important dans le maintien de l’intégrité du génome, mais dans la plupart des cellules de notre corps, les télomères deviennent plus courts à chaque division cellulaire puisque l’activité de l’enzyme de maintenance des télomères (TERT) est progressivement réprimée. Après un raccourcissement suffisant des télomères, leur fonction protectrice est perdue, activant le gène suppresseur de tumeur p53 et la réponse aux dommages à l’ADN. Cela conduit à un état non prolifératif appelé sénescence dans les cellules normales, ou à la mort cellulaire dans les cellules cancéreuses. On pense que ces effets inhibiteurs sur la prolifération cellulaire sont un mécanisme important pour empêcher la prolifération de cellules endommagées et la formation de tumeurs.
![]()
-
26 April 2021 Une levure pathogène a plusieurs tours dans son sac
Les infections par la levure Candida albicans constituent un problème de santé publique important et une complication commune chez les individus immunodéprimés comme les sidéens, les patients en chimiothérapie et les patients ayant subi une transplantation d’organe. Bien qu’il existe certains traitements, leur efficacité peut être compromise par l’apparition de souches résistantes et l’identification de nouveaux antifongiques est hautement désirable. Or, il y a quelques années, une équipe de l’IRIC a identifié la nicotinamide (NAM), une forme de la vitamine B3, comme un traitement antifongique potentiel.
![]()
-
21 April 2021 Conférence de Guy Sauvageau à la CCMM: entre innovation, recherche et philanthropie
En conférence à la Chambre de commerce du Montréal métropolitain, Guy Sauvageau a annoncé la création d’une chaire de recherche en chémogénomique des cellules souches sanguines.
![]()
-
13 April 2021 La coordination spatiotemporelle: un aspect clé permettant aux cellules de se diviser correctement
Les enzymes régulatrices de la division cellulaire doivent être soumises à un contrôle spatiotemporel leur permettant d’accéder aux structures cellulaires qu’elles contrôlent seulement au moment opportun. La ségrégation des chromosomes durant la mitose est l’événement le plus crucial de la division cellulaire. La coordination spatiotemporelle est donc fondamentale au bon déroulement de la mitose.
![]()
-
1st April 2021 TMEM16F: une protéine avec un rôle clé dans la régulation de l’activité des lymphocytes T
Par Fatéma Dodat
Comprendre la régulation de l’activité des cellules T représente un enjeu crucial pour le développement d’une immunité contre les infections, mais aussi dans le cancer. Une étude menée par l’équipe du chercheur Etienne Gagnon révèle que TMEM16F, une molécule favorisant l’échange des constituants entre les feuillets de la bicouche lipidique d’une membrane cellulaire, est impliquée dans cette activation.
![]()
-
30 March 2021 Un pas de plus est franchi vers un vaccin anticancer
Claude Perreault et son équipe publient cette semaine un article important sur la mise au point d’un vaccin thérapeutique contre un cancer du sang.
![]()
-
26 February 2021 L’IRIC entrevoit un traitement pour l’obésité sévère
Par Mathieu-Robert Sauvé, UdeM Nouvelles
Michel Bouvier présente son étude sur une piste de traitement pour une forme d’obésité d’origine génétique.
![]()
-
17 February 2021 Michel Bouvier, DG de l’IRIC, participe au symposium pancanadien sur l’avenir de la découverte et la production de médicaments au Canada
L’Institut de recherche en immunologie et cancérologie (IRIC) de l’Université de Montréal est fier d’annoncer la participation de Michel Bouvier, Directeur général de l’Institut, récemment récipiendaire du prix Killam en sciences de la santé, à l’événement virtuel « Building Biotech : Science and Talent Accelerating Biomedical Innovation, a Pan-Canadian Showcase and Dialogue ». Ce symposium a lieu aujourd’hui, le 17 février 2021 et est organisé par PRiME à l’Université de Toronto.
![]()
-
4 February 2021 Journée mondiale contre le cancer 2021 : Aidez-nous à vaincre le cancer!
La Journée mondiale contre le cancer est célébrée annuellement, le 4 février, aux quatre coins du globe. Elle permet de souligner les incroyables avancées de la recherche contre le cancer qui permettent de sauver de plus en plus de vies et génèrent un espoir indéniable. En souvenir de ceux qu’on aime qui sont partis trop tôt ou en hommage à ceux qui luttent actuellement contre la maladie, soulignons ensemble cette Journée, le progrès que nous avons fait et celui qu’il nous reste à parcourir.
![]()
-
3 February 2021 Michel Bouvier est récipiendaire du prix Killam 2021 en sciences de la santé
Michel Bouvier, Directeur général de l’IRIC et Professeur au Département de biochimie et médecine moléculaire de la Faculté de médecine de l’Université de Montréal, est récipiendaire du prix Killam 2021 en sciences de la santé.
![]()
-
26 January 2021 Bourses de maîtrise et de doctorat de l’IRIC – Récipiendaires du Concours Automne 2020
À l’issue du Concours de bourses de maîtrise et de doctorat de l’IRIC tenu cet automne, l’Institut est fier d’annoncer les 17 récipiendaires de cette édition.
![]()
-
12 January 2021 La molécule UM171 continue de donner des résultats encourageants
L’équipe de Guy Sauvageau a publié un article démontrant le mécanisme d’action de la molécule UM171.
![]()
-
2 December 2020 Nanotechnologies : l’équipe du laboratoire Bouilly relève des principes importants dans la conception des biocapteurs
Au cours de la dernière décennie, les progrès dans le domaine des nanotechnologies, en particulier la découverte de nouveaux nanomatériaux, ont catalysé des innovations remarquables dans la création de différents biocapteurs, c’est à dire des dispositifs d’analyse permettant de détecter et d’étudier les propriétés de nombreuses molécules biologiques. Il existe de nombreux types de biocapteurs et il est souvent difficile de comparer leurs performances et d’identifier les approches les plus prometteuses.
![]()
-
9 November 2020 Le projet de Sébastien Lemieux et de son équipe est récipiendaire du concours DOCC
Génome Québec, IVADO et l’Oncopole se sont réuni pour organiser le concours « Données omiques contre le cancer » (DOCC). Cette initiative vise à soutenir des projets développant des applications et des outils d’intelligence artificielle utilisés pour mieux exploiter les ensembles de données générées par la génomique et l’étude du cancer.
Le projet de Sébastien Lemieux, chercheur principal à l’IRIC et de son équipe fait partie des 5 projets récipiendaires du programme.
![]()
-
20 October 2020 L’équipe des affaires académiques de l’IRIC reçoit le prix d’excellence en enseignement
L’IRIC est fier d’annoncer l’obtention du prix d’excellence en enseignement Catégorie Innovation – Soutien à la réussite étudiante par son équipe des affaires académiques : Sébastien Carréno, Julie Mantovani, Evelyne Muhire, Pascale Le Thérizien. Cette reconnaissance attribuée par le Vice-rectorat aux affaires étudiantes et aux études de l’Université de Montréal souligne la contribution exceptionnelle de l’équipe au soutien à la réussite étudiante.
![]()
-
15 October 2020 Tournée de recrutement étudiant 2020 : une édition virtuelle cet automne
L’équipe des affaires académiques de l’IRIC lance chaque automne une tournée de recrutement étudiant « IRIC sur la route ». Cette année, dans le contexte exceptionnel engendré par la pandémie de COVID-19, nos représentantes partent à la rencontre des étudiant.e.s virtuellement. Elles participeront à plusieurs salons d’études supérieures organisés sur la toile par diverses universités canadiennes.
![]()
-
14 October 2020 Un soutien au bénéfice de l’IRIC et du Département de biochimie et médecine moléculaire de l’UdeM
Dans le cadre d’une vaste campagne de dons planifiés menée par le Réseau des diplômés et des donateurs de l’Université de Montréal, Michel Bouvier, directeur général de l’IRIC et sa conjointe, Muriel Aubry, se sont engagés à faire un leg testamentaire au profit de l’Institut et du Département de biochimie et médecine moléculaire de l’UdeM pour soutenir la recherche contre le cancer et la formation de la relève scientifique.
![]()
-
13 October 2020 Rompre le paradigme de la coiffe de l’ARN
Cette découverte d’une équipe de chercheurs de l’IRIC pourrait bientôt être enseignée dans les cours de biologie moléculaire. Le laboratoire de Katherine Borden a récemment publié une étude dans la revue PNAS qui démontre que l’activité des ARN peut être régulée d’une nouvelle manière: en modulant une modification de l’ARN appelée « capping ».
![]()
-
4 September 2020 Trois chercheurs de l’IRIC reçoivent un appui substantiel de la Fondation canadienne pour l’innovation
Le 18 août 2020, la Fondation canadienne pour l’innovation (FCI) a annoncé les projets de recherche sélectionnés qui bénéficieront de son soutien financier. Cet appui substantiel permet notamment aux chercheuses et chercheurs de s’outiller en équipements hautement spécialisés et locaux avant-gardistes, et de recruter et maintenir en poste des scientifiques réputés.
![]()
-
6 August 2020 Des cribles pangénomiques revèlent que le resvératrol induit un stress réplicatif sur les cellules humaines
Le resvératrol (RSV) est un composé naturel présent dans de nombreuses plantes, y compris la peau des raisins (et du vin), les myrtilles, les framboises, les mûres et les arachides. Il a beaucoup attiré l’attention des chercheurs en raison de ses propriétés bénéfiques rapportées dans des modèles expérimentaux tels que les levures, les vers nématodes, les mouches des fruits et les souris, y compris l’allongement de la durée de vie dans certaines conditions. Un rôle causal du RSV dans la santé humaine n’a pas encore été établi.
![]()
-
29 September 2022 Des jeunes mettent sur pied une collecte de fonds pour l’IRIC
L’IRIC souligne l’acte de générosité du Collège Nouvelles Frontières. Lors d’une de leurs « journées civiles payantes » où les élèves obtiennent le droit de troquer leur uniforme pour les vêtements de leur choix, ces derniers profitent également de cette journée attendue pour amasser des fonds pour soutenir la communauté.
-
13 May 2022 SQSV 2022-2025 : Des nouvelles encourageantes pour l’industrie!
L’IRIC se réjouit de l’annonce du ministre de l’Économie et de l’Innovation du Québec, monsieur Pierre Fitzgibbon, quant au dévoilement de la Stratégie québécoise des sciences de la vie 2022-2025 dans le cadre de l’événement phare Effervescence. Sous le thème « Utiliser notre ingéniosité pour faire évoluer la santé », la stratégie, mise à jour dans le contexte de la COVID-19, propose des actions concrètes et innovantes pour valoriser cette industrie clé de l’économie du Québec et en favoriser l’essor.
-
12 April 2022 Journée mondiale de la santé : Contribuons à notre avenir collectif
Le 7 avril dernier avait lieu la Journée mondiale de la santé, qui vise cette année à souligner l’importance de préserver la santé des êtres humains et de la planète; une occasion pour l’IRIC de réitérer l’apport inestimable de ses donateurs et donatrices.
-
24 January 2022 Investir dans la recherche : un geste qui rapporte
Un éventuel vaccin thérapeutique contre le cancer des ovaires, un nouveau traitement contre la leucémie et une molécule qui pourrait même court-circuiter jusqu’à 70 % de tous les types de cancers… Ces trois projets en cours de développement à l’IRIC ont bénéficié de fonds provenant de donations privées. Parmi ceux-ci, les titres cotés en bourse constituent une façon avantageuse de contribuer à la prochaine génération de traitements contre le cancer.
-
17 January 2022 Ciné-conférence: Le cancer pédiatrique : un accompagnement scientifique et humain
L’IRIC en collaboration avec la Faculté de médecine et le réseau des diplômés et des donateurs de l’UdeM offriront une édition spéciale des Ciné-conférences le 3 février 2021, dans le cadre de la Journée mondiale contre le cancer.
-
7 October 2021 L’IRIC accueille deux nouveaux agents de communication
Nous sommes heureux de vous annoncer l’entrée en poste de Thomas Milan (27 septembre) et de Myreille Larouche (14 octobre) au poste d’agents de communication et relations médias. L’IRIC a à cœur d’encourager sa relève. Nous sommes ainsi fiers et enthousiastes à l’idée d’avoir deux scientifiques, dotés de grandes aptitudes communicationnelles, comme nouveaux ambassadeurs de l’Institut.
-
4 October 2021 -
22 September 2021 Tournée de recrutement étudiant 2021 : une édition de nouveau virtuelle cet automne
L’équipe des affaires académiques de l’IRIC lance chaque automne une tournée de recrutement étudiant « IRIC sur la route ». Cette année, nos représentantes partent à la rencontre des étudiant.e.s virtuellement. Elles participeront à plusieurs salons d’études supérieures organisés sur la toile par diverses universités canadiennes.
-
19 July 2021